La science explique la maladie rare qui transforme lentement ses victimes en « pierre »

Il existe toute une liste de troubles génétiques courants, tels que les troubles du spectre autistique, le cancer, le diabète, le syndrome de Down et le spina bifida. Comme il y a (apparemment) moins de maladies rares, elles sont moins connues. Certaines d’entre elles n’ont jamais été évoquées car elles touchent très peu de personnes. Avec une prévalence de moins d’une personne sur 1 million aux États-Unis (d’après une recherche publiée dans Orphanet Journal of Rare Diseases), la « maladie de l’homme de pierre » en est un exemple.
Médicalement appelée fibrodysplasie ossifiante progressive (FOP), les scientifiques savent depuis 2006 que cette maladie rare implique presque toujours une mutation d’un gène appelé récepteur de l’activine A de type 1 (ACVR1) et ont publié leurs résultats dans Nature Genetics. Ce gène spécifique « code pour un récepteur de protéine morphogénique osseuse (BMP) de type I », comme décrit dans Biomedicines. Dans la présentation classique de la FOP, l’acide aminé arginine remplace l’acide aminé histidine, qui active le gène muté. Cela déclenche un processus appelé ossification hétérotopique (HO), qui implique la croissance des os dans les tissus mous, notamment les muscles, les ligaments et les tendons, là où ils ne le feraient normalement pas.
Bien que cette croissance osseuse extrasquelettique puisse survenir après tout type de blessure et soit généralement si petite qu’elle ne provoque pas de symptômes, il s’agit plutôt d’un processus continu dans la FOP. Tout type de traumatisme, comme une chute ou une intervention chirurgicale, peut provoquer une poussée d’inflammation et de gonflement qui peut durer plusieurs mois. Même la grippe ou une autre maladie non physiquement traumatisante peut provoquer une poussée. Au fil du temps, les tissus mous se transformant en os limitent l’amplitude des mouvements et deviennent débilitants.
Le diagnostic et le traitement de la fibrodysplasie ossifiante progressive sont difficiles
Même si la survenue de la FOP peut être évidente chez certaines personnes, ce n’est pas toujours le cas. Avoir des gros orteils anormalement gros (hallux valgus) à la naissance peut être un indicateur utile. Cependant, en général, le processus HO commence dès la petite enfance au niveau du cou et des épaules et finit par se déplacer vers d’autres zones du corps. L’os extrasquelettique peut croître rapidement ou lentement, cette dernière pouvant rendre le diagnostic plus difficile. En fait, les erreurs de diagnostic sont fréquentes car cette maladie est rare et partage certaines similitudes avec d’autres problèmes de santé.
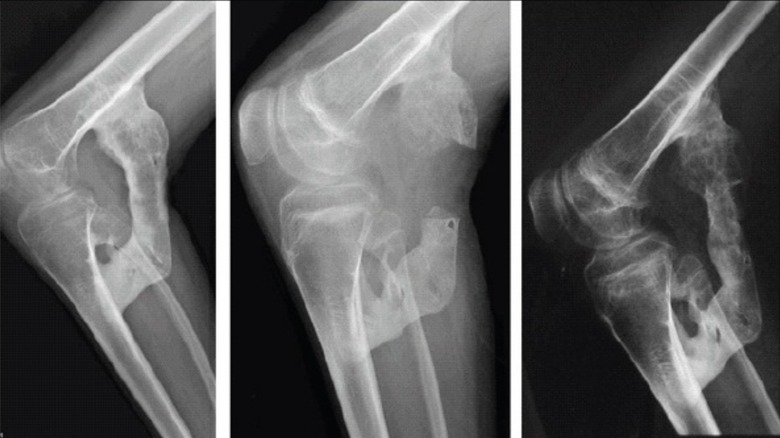
Outre un examen physique (en particulier les orteils) et des techniques d’imagerie telles que les rayons X pour évaluer la nouvelle croissance osseuse, le diagnostic de la FOP comprend souvent l’identification des symptômes et l’examen des antécédents médicaux familiaux. Les médecins n’effectueront pas de biopsie diagnostique s’ils soupçonnent que le problème de santé est la FOP, car la procédure invasive peut provoquer une poussée. Au lieu de cela, ils ordonnent généralement le séquençage du gène ACVR1 pour déterminer si la mutation désavantageuse s’est produite ou non.
Étant donné qu’environ 800 personnes seulement dans le monde sont atteintes de FOP (selon le Centre d’information sur les maladies génétiques et rares), il n’existe pas encore de traitement solide. Éviter les poussées grâce à une antibiothérapie préventive et gérer la douleur et l’enflure avec des médicaments sont les principaux moyens de traiter cette maladie.
Les agences de réglementation d’Australie, du Canada et des États-Unis ont approuvé un agoniste sélectif du récepteur gamma de l’acide rétinoïque (RARγ) appelé Palovarotène pour inhiber la nouvelle formation de HO (selon une étude publiée dans Journal of Bone and Mineral Research Plus). Cependant, il ne réduit que partiellement la nouvelle formation de HO, présente une toxicité potentielle et est associé à des effets secondaires importants. Comme l’ont souligné les scientifiques dans une étude publiée dans Biomedicines, la recherche d’autres traitements efficaces est en cours, et certains sont en cours d’essais cliniques.